铁死亡是一种与已知的其它调控性细胞死亡有本质区别的二价铁离子依赖的细胞死亡模式,由于其能够调控细胞内氧化还原平衡状态,对肿瘤干细胞和具有上皮间质转化特征的耐药细胞具有毒性作用,近年来被广泛用于肿瘤治疗。然而,并非所有类型的肿瘤细胞均对这一机理敏感,即铁死亡具有细胞选择性。铁死亡的肿瘤细胞选择性涉及多种机理,其中细胞内长链脂酰辅酶A合成酶4 (ACSL4) 的低表达或无表达是一个重要因素,ACSL4是铁死亡级联过程的关键酶,对生成细胞铁死亡的致死信号,即花生四烯酸-磷脂酰乙醇胺 (PE-AA) 的过氧化物至关重要。
近日,药学院赵燕军和王征教授团队针对ACSL4 缺乏导致的铁死亡细胞选择性问题,选择了ACSL4缺乏的MCF-7乳腺癌细胞为模型,利用两亲性二茂铁高分子胶束来共递送PE-AA和硫氧还蛋白还原酶抑制剂 (金诺芬) (图1)。二茂铁高分子具有过氧化氢敏感特性,在肿瘤细胞微环境内可实现活性分子和铁离子的可控释放,PE-AA 的直接递送在细胞和荷瘤动物水平显著提高了铁死亡对ACSL4缺失细胞的毒性作用。这一工作为解决铁死亡的肿瘤细胞选择性问题提供新思路与新方法。
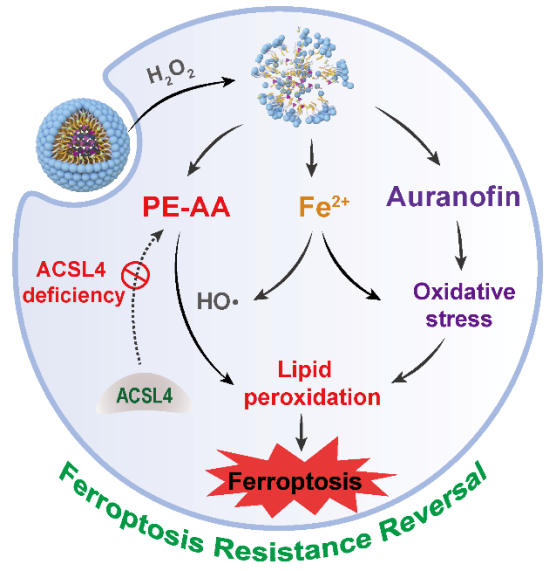
图1. 高分子共递送胶束逆转ACSL4缺乏导致的铁死亡耐药示意图
相关研究成果以“Reversing Ferroptosis Resistance in Breast Cancer via Tailored Lipid and Iron Presentation” 为题发表在《ACS Nano》杂志,天津大学是第一作者单位,这一工作主要由药学院研究生罗佳佳完成,该工作得到了天津医院合作团队和天津大学药学院分析中心的大力支持和帮助。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.3c08485


