肝纤维化作为由多种慢性肝损伤诱发的渐进性病理改变,是肝硬化、肝功能衰竭和肝细胞癌的关键风险因素。在病理进程中,静息肝星状细胞(quiescent hepatic stellate cells, qHSCs)向活化表型(activated HSCs, aHSCs)的转化构成了纤维化发展的核心驱动力,该转变过程伴随显著的细胞能量代谢重编程和细胞外基质的过量产生。鉴于aHSCs在纤维形成中的主导地位,该类细胞已成为抗纤维化治疗的关键靶细胞。然而,aHSCs与邻近qHSCs间的病理性细胞间通讯的增强会持续驱动后者活化,从而导致治疗效率受限。
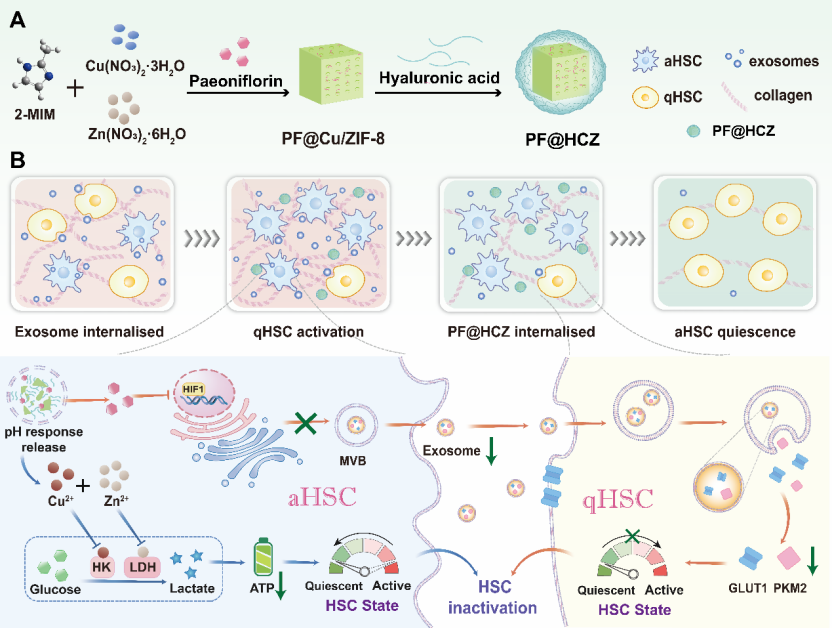
李楠教授团队长期致力于肝纤维化治疗研究,其多篇论文(Adv. Mater.2024, 2406590; Adv. Func. Mater. 2024, 2309690; Acta. Pharm. Sin. B, 2023,13 (12): 5030-5047)深入探究肝纤维化演进的多种机制及潜在靶点,并从不同角度提出创新治疗策略。本研究开发了新型细胞间通讯干扰治疗策略,构建了特异性靶向aHSCs的芍药苷负载铜掺杂ZIF-8纳米材料(PF@HA-Cu/ZIF-8, PF@HCZ)。该纳米系统通过双重机制实现抗纤维化效应:① 靶向抑制aHSCs能量代谢相关外泌体分泌,阻断对邻近qHSCs的活化诱导;② 通过释放的Cu2?/Zn2?抑制糖酵解关键酶活性,减少生物能量合成,促使aHSCs恢复静息表型,进而协同降低外泌体及细胞外基质分泌。研究表明,PF@HCZ能够通过维持aHSCs与qHSCs的代谢休眠状态,最终显著缓解肝纤维化病理进程。这一发现为通过靶向细胞间通讯和重塑代谢稳态的抗纤维化治疗提供了创新性策略。
相关研究成果以“Intercellular communication interference through energy metabolism-related exosome secretion inhibition for liver fibrosis treatment”为题,发表于中国科技期刊卓越行动计划领军期刊《Acta Pharmaceutica Sinica B》,天津大学医学部药学院为论文第一通讯单位,李楠教授为最后通讯作者,2022级硕士研究生张梦瑶为第一作者。本研究工作得到了药学院仪器测试中心的大力支持和帮助,并受到国家自然科学基金面上项目、天津市自然科学基金重点项目和天津市青年科技人才项目的资助。


